药用精氨酸原厂5kg起订制药辅料L-精氨酸符合中国药典标准医药级盐酸精氨酸原料全套资质
生产许可证
注册批件
质量标准
出厂质检单COA
药典标准
有备案登记
精氨酸
来源:二部 分类:正文品种第一部分 页码:1510
L-精氨酸 CAS#: 74-79-3
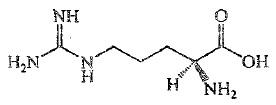
C6H14N4O2 174.20
本品为L-2-氨基-5-胍基戊酸。按干燥品计算,含C6H14N4O2不得少于99.0%。
【性状】本品为白色结晶或结晶性粉末,几乎无臭,有特殊味。
本品在水中易溶,在乙醇中几乎不溶;在稀盐酸中易溶。
比旋度 取本品,精密称定,加6mol/L盐酸溶液溶解并定量稀释制成每1ml中约含80mg的溶液,依法测定(通则0621),比旋度为+26.9°至+27.9°。
【鉴别】 (1)取本品与精氨酸对照品各适量,分别加0.1mol/L盐酸溶液溶解并稀释制成每1ml中约含10mg的溶液,作为供试品溶液与对照品溶液。照其他氨基酸项下的色谱条件试验,供试品溶液所显主斑点的位置和颜色应与对照品溶液的主斑点相同。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集1075图)一致。
【检查】 碱度 取本品2.5g,加水25ml溶解后,依法检查(通则 0631),pH值应为10.5~12.0。
溶液的透光率 取本品1.0g,加水10ml溶解后,照紫外-可见分光光度法(通则0401),在430nm的波长处测定透光率,不得低于98.0%。
氯化物 取本品0.30g,依法检查(通则0801),与标准氯化钠溶液6.0ml制成的对照液比较,不得更浓(0.02%)。
硫酸盐 取本品1.0g,依法检查(通则0802),与标准硫酸钾溶液2.0ml制成的对照液比较,不得更浓(0.02%)。
铵盐 取本品0.10g,依法检查(通则0808),与标准氯化铵溶液2.0ml制成的对照液比较,不得更深(0.02%)。
蛋白质 取本品1g,加水10ml溶解后,加20%三氯醋酸溶液5滴,不得生成沉淀。
其他氨基酸 取本品适量,加0.1mol/L盐酸溶液溶解并稀释制成每1ml中约含10mg的溶液,作为供试品溶液;精密量取1ml,置250ml量瓶中,用0.1mol/L盐酸溶液稀释至刻度,摇匀,作为对照溶液;另取精氨酸对照品与盐酸赖氨酸对照品各适量,置同一量瓶中,加0.1mol/L盐酸溶液溶解并稀释制成每1ml中分别约含精氨酸10mg和盐酸赖氨酸0.4mg的溶液,作为系统适用性溶液。照薄层色谱法(通则0502)试验,吸取上述三种溶液各5μl,分别点于同一硅胶G薄层板上,以正丙醇-浓氨溶液(6:3)为展开剂,展开约20cm后,晾干,在90℃干燥约10分钟,放冷,喷以1%茚三酮的正丙醇溶液,在90℃加热至斑点出现,立即检视。对照溶液应显一个清晰的斑点,系统适用性溶液应显两个完全分离的斑点。供试品溶液如显杂质斑点,不得超过1个,其颜色与对照溶液的主斑点比较,不得更深(0.4%)。
干燥失重 取本品,在105℃干燥3小时,减失重量不得过0.5%(通则 0831)。
炽灼残渣 不得过0.1%(通则0841)。
铁盐 取本品1.0g,依法检查(通则0807),与标准铁溶液1.0ml制成的对照液比较,不得更深(0.001 %)。
重金属 取本品1.0g,加水23ml与醋酸盐缓冲液(pH 3.5)2ml溶解后,依法检查(通则0821 第一法),含重金属不得过百万分之十。
砷盐 取本品2.0g,加水23ml溶解后,加盐酸5ml,依法检查(通则0822 第一法),应符合规定(0.0001%)。
细菌内毒素 取本品,依法检查(通则1143),每1g精氨酸中含内毒素的量应小于10EU。(供注射用)
【含量测定】 取本品约80mg,精密称定,加无水甲酸3ml使溶解后,加冰醋酸50ml,照电位滴定法(通则0701) ,用高氯酸滴定液(0.1mol/L)滴定,并将滴定的结果用空白试验校正。每1ml高氯酸滴定液(0.1mol/L)相当于8.710mg的C6H14N4O2。
【类别】 氨基酸类药。
【贮藏】 密封保存。




